이주형의 식품수출 실전노트 20. 기능성표시식품 실무 가이드①

법무법인 광화문
작년까지는 SR만 챙기면 됐는데
“저희가 일본 파트너사와 프로바이오틱스 기능성표시식품 신고를 준비하고 있는데요, 작년까지는SR이랑 표시안만 챙기면 된다고 했거든요. 그런데 올해 들어서 갑자기GMP 적합 서류, 건강피해 정보 수집 체계도, 자기점검 보고 일정까지 묻습니다. 대체 뭐가 바뀐 건가요?”
최근 일본향 기능성표시식품 신고를 준비하는 한국 기업에서 이런 질문을 자주 받습니다. 프로바이오틱스, 루테인, 콜라겐 같은 원료로 일본 시장을 노크하던 업체들이, 어느 순간부터 서류 목록이 두꺼워진 것을 체감하고 있는 겁니다.
이유는 하나입니다. 2024년3월, 고바야시제약(小林製薬)의 홍국(紅麹) 서플리먼트에서 대규모 건강피해가 발생했습니다. 이 제품은 기능성표시식품으로 신고되어 판매되고 있었고, 섭취자 중 신장 장해 등 심각한 증상이 다수 보고되었습니다. 문제는 피해 규모만이 아니었습니다.
고바야시제약은 2024년1월에 의사로부터 건강피해 정보를 처음 제공받았으나, 내부에서 원인을 규명하려다 소비자청과 오사카시에 보고하기까지 약 2개월이 걸렸습니다. 만약 섭취를 빨리 중단하도록 행정이 개입했다면 피해가 줄었을 것이라는 비판이 쏟아졌습니다.후생노동성은 국립의약품식품위생연구소 등과 함께 원인물질 규명에 착수했고, 2024년 5월 말까지 밝혀진 사실은 다음과 같습니다. 건강피해가 집중된 원료 로트에서 푸베루산(プベルル酸) 외에 모나콜린K와 기본 골격이 유사한 2종의 화합물이 확인되었고, 공장 내 청색 곰팡이(Penicillium adametzioides)가 배양 단계에서 혼입하여 이 물질들을 생성한 것으로 추정되었습니다. 환자의 약8할은 해당 제품 섭취를 중단하자 증상이 개선되는 경향을 보였습니다.
이 사안 하나가, 일본 기능성표시식품 제도를 근본적으로 바꿔놓았습니다. 기존에는 “사업자 책임으로 신고하고 표시하는” 제도였다면, 개편 후에는 “제조관리+신고+표시+사후감시”가 결합된 운영 체계로 전환되었습니다. 이 편에서는 그 전체 그림을 그리겠습니다.
한국 건강기능식품≠일본 기능성표시식품
한국의 “건강기능식품”과 일본의 “기능성표시식품”은 이름만 비슷할 뿐, 제도 구조가 근본적으로 다릅니다. 이 차이를 먼저 짚지 않으면 이후의 모든 실무가 엇나갑니다.
일본에서 건강에 관한 기능성을 표시할 수 있는 식품은 보건기능식품(保健機能食品)이라는 상위 범주 안에 세 가지로 나뉩니다.
첫째, 특정보건용식품(特定保健用食品)은 국가(소비자청)가 개별 심사ㆍ허가하는 제도입니다. 한국 건강기능식품의 개별인정형과 가장 가깝습니다.
둘째, 기능성표시식품(機能性表示食品, FFC)은 사업자가 안전성ㆍ기능성의 과학적 근거를 갖추어 소비자청 장관에게 신고하면 기능성을 표시할 수 있는 제도입니다. 국가의 개별 심사를 거치지 않는다는 점에서 특정보건용식품과 근본적으로 다릅니다.
셋째, 영양기능식품(栄養機能食品)은 규격이 정해진 비타민ㆍ미네랄에 한해 별도 신고 없이 기능을 표시할 수 있는 제도입니다.
핵심은 “사업자 책임”이라는 네 글자입니다. 한국에서 식약처 허가를 받은 건강기능식품 원료라 하더라도, 일본에서는 기능성표시식품 신고 시 자체적으로 안전성ㆍ기능성 근거를 갖춰야 합니다. 한국 허가를 일본 신고로 “이관”하는 절차는 존재하지 않습니다.
한국에서 식약처 인정을 받은 원료라도 일본 기능성표시식품 신고를 위해서는 별도의 증빙 체계가 필요합니다.
홍국 사안 이후, 무엇이 바뀌었나 - 4가지 변화
2024년 5월 31일, 일본 정부는 관계각료회의(紅麹関連製品への対応に関する関係閣僚会合)를 열어 기능성표시식품 제도의 향후 대응 방향을 확정했습니다. 이 결정이 이후 모든 법령 개정의 출발점입니다. 핵심은4개의 축으로 나뉘며, 각각 시행 시점이 다릅니다.
변화1: 건강피해 정보 제공 의무화(2024년 9월 1일 즉시 시행)
홍국 사안에서 가장 문제가 된 것은 “보고 지연”이었습니다. 기존에는 기능성표시식품 가이드라인에서 “건강피해의 발생 및 확대 우려가 있는 경우” 소비자청에 보고하도록 되어 있었지만, 사업자가 내부적으로 인과관계를 판단한 뒤 보고하는 구조였기 때문에 시간이 걸렸습니다.
개정 후에는 구조 자체가 바뀌었습니다. 신고자(届出者)는 건강피해로 의심되는 정보를 수집해야 하며, 의사가 진단한 건강피해 정보를 파악한 경우에는 해당 식품과의 인과관계가 불명확하더라도 신속하게 도도부현 지사 등 및 소비자청 장관에게 정보를 제공해야 합니다. 식품표시법상 신고자 준수사항과 식품위생법상 정보제공 의무가 맞물리면서, “내부 평가 후 보고”에서 “신속 정보 제공” 중심 구조로 전환된 것입니다.
한국 본사가 일본 파트너로부터 “건강피해 정보 수집 체계도를 보여달라”는 요구를 받는 것은 이 의무화 때문입니다. 일본 파트너가 신고자라면, 법적으로 건강피해 정보를 수집하고 신속 제공해야 할 의무가 있고, 제조사인 한국 기업에게도 정보 흐름을 요구할 수밖에 없습니다.
구체적인 보고 요건 - 동일 소 견2건 발생 시 15일 이내, 중증 사례는 1건이라도 15일 이내 - 은 후생노동성ㆍ소비자청이 별도 통지에서 정하고 있으며, 실무상 한국CS팀→일본 파트너→보건소ㆍ소비자청으로 이어지는 정보 경로를 사전에 설계해 두어야 합니다. 이 체계의 설계 방법은24편에서SOP 템플릿과 함께 다루겠습니다.
변화2: 제도 신뢰성 강화 - GMPㆍ표시ㆍ전문가 의견 청취(2025년4월 시행/ GMP 경과조치2026년 8월 31일)
(1) GMP 요건화
천연추출물 등을 원재료로 하는 정제ㆍ캡슐형 식품에 대해GMP(적정제조규범) 기준에 따른 제조관리가 신고자의 준수사항으로 식품 표시기준에 규정되었습니다. 구체적인 기준은 내각부 고시 제108호로 공포되었고, 경과조치 기간은 2026년 8월 31일까지입니다. 2026년 9월 1일부터는 이 기준을 준수하지 않으면 기능성표시식품으로서의 요건을 충족하지 못하게 됩니다.
모든 기능성표시식품이GMP 대상은 아닙니다. 대상은 식품표시기준상 “천연추출물 등을 원재료로 하는 정제ㆍ캡슐형 식품”으로 신고한 경우입니다. 통상 이 범주에 해당하지 않는 일반 가공식품(음료, 과자 등)은 직접적인GMP 의무 대상이 아닙니다. 다만 소비자청의 신고 안내서에서는 기타 가공식품에 대해서도GMP 인증, HACCP, ISO22000, FSSC22000 등의 인증 유무를 신고 시 기재하도록 하고 있어, 제조관리 전반에 대한 기대 수준이 올라가고 있는 것은 분명합니다.
한국 건강기능식품GMP를 갖추고 있다고 해서 일본 고시 기준에 자동 적합한 것은 아닙니다. 일본 고시는 총괄책임자ㆍ제조관리책임자ㆍ품질관리책임자의 3자 분리, 제품표준서ㆍ제조관리기준서ㆍ품질관리기준서ㆍ수순서4종 문서 체계, 밸리데이션, 일탈관리, 변경관리, 원재료의 안전성 정보 수집 등을 요구합니다. 한국GMP를 갖추고 있다면 출발점은 유리하지만, 갭 분석이 반드시 필요합니다.
제가 자문한 업체들의 경험상GMP 체계 정비에는 갭 분석부터 문서 정비, 현장 적용까지6개월에서1년 정도 소요되는 경우가 많았습니다. 2026년9월 시한까지 남은 시간이 약5개월입니다. 아직 착수하지 않은 기업이라면, 지금이 마지막 타이밍입니다. 고시 조문 단위의 대조와 한국 GMP와의 차이 분석은 21편에서 다루겠습니다.
(2) 표시 방식 개정
기능성표시식품의 표시 방식이 크게 개정되었습니다. 용기포장의 주요면 상단에 “기능성표시식품(機能性表示食品)”이라는 문자를 테두리 상자로 둘러싸서 표시해야 하고, 신고번호를 해당 표시에 근접한 위치에 기재해야 합니다. “특정보건용식품과 달리 안전성 및 기능성에 대해 국가의 평가를 받은 것이 아닙니다”라는 취지의 문구도 개정되었고, 신고 표시 내용의 발췌는 금지되었으며, 의약품과의 상호작용ㆍ과잉섭취 주의사항을 과학적 근거에 기반하여 구체적으로 기재해야 합니다.
일본 기능성표시식품의 라벨은 이제 “문구를 넣는” 수준이 아니라, 소비자가 전면표시와 신고DB 정보를 연결해 읽도록 설계되는 표시체계로 바뀌고 있습니다. 한국 건강기능식품 라벨을 일본어로 번역하는 방식으로는 대응이 불가능하며, 일본 표시 규정에 맞춘 재설계가 필요합니다. 특히 마케팅팀과 QA팀이 동시에 움직여야 하는 영역입니다. 표시 개정의 구체적인 체크리스트와 레이아웃 설계 포인트는 23편에서 다루겠습니다.
(3) 전문가 의견 청취 구조 도입
신규 기능성관여성분에 대해서는, 소비자청이 신고 자료의 안전성ㆍ기능성 과제에 대해 의학ㆍ약학 등 과학적 지견을 가진 전문가의 의견을 듣는 구조가 도입되었습니다. 이에 따라 기존에 공표된 적 없는 기능성관여성분이나 조합 등으로 자료 확인에 특히 시간이 필요하다고 소비자청 장관이 인정하는 경우, 예외적으로120영업일 전 신고 구조가 적용될 수 있습니다. 이 변화는22편에서 상세히 다루겠습니다.
변화3: 신고ㆍDBㆍ자기점검 운영 재정비(2025년 4월 1일 시행)
2025년 4월 1일을 기점으로 기능성표시식품의 신고 운영 체계가 대폭 정비되었습니다.
(1) 신고 확인기간 변경
기존 판매 개시일 60일 전→60영업일 전으로 변경되었고, 기존에 공표된 적 없는 기능성관여성분이나 조합 등으로 자료 확인에 특히 시간이 필요하다고 소비자청 장관이 인정하는 경우에는 예외적으로 120영업일 전 신고 구조가 적용될 수 있습니다. 다만 새로운 헬스클레임이라는 이유만으로 120영업일이 되는 것은 아니며, 핵심은 ‘기존 공표 이력’과 ‘자료 확인 난이도’입니다. 기본은 60영업일이고, 120영업일은 예외적 특례입니다.
(2) 과학적 근거 질 향상
시스테마틱 리뷰(SR)의 보고 가이드라인으로PRISMA 2020의 준거가2025년4월 이후 신규 신고에 필수화되었습니다. 기존에 신고된 기능성표시식품에 대해서도 재검토가 권고되고 있습니다.
(3) 자기점검ㆍ보고 의무화
신고자가 준수사항을 이행하고 있는지 정기적(연1회)으로 자기점검하고, 그 결과를 신고DB를 통해 보고해야 합니다. 기한 내 보고하지 않으면 해당 신고는 기능성표시식품으로서의 요건을 결하게 되며, DB상 변경신고ㆍ판매상황 갱신ㆍ철회 등 후속 작업도 제한됩니다.
(4) 신고DB 개편
2025년4월부터 기능성표시식품 신고 데이터베이스는 G비즈 ID(GビズID, 일본 정부 공통 사업자 인증 시스템) 대응 체계로 운영되고 있습니다. 신규 이용 사업자는 G비즈 ID 취득이 필요하고, 기존 사업자ID 보유자는 G비즈 ID와 연동하여 전환할 수 있습니다(단, 연동 후에는 기존 ID 사용 불가). 따라서 일본 현지 신고자가 실제 신고ㆍ변경ㆍ자기점검 보고를 수행할 수 있는 로그인 및 권한 체계를 확보했는지 확인해 둘 필요가 있습니다.
한국에서 이미 많이 쓰는 원료라도 일본 소비자청이 “신규 성분”으로 분류하면120영업일이 적용될 수 있어, 출시 일정이 반년 가까이 밀리는 경우가 생깁니다. 한국 식약처의 개별인정형 허가와 일본 소비자청의 신규/기존 판단은 완전히 별개입니다. 또 PRISMA 2020 대응은 기존 방식의 SR을 그대로 쓸 수 없다는 뜻이기도 합니다. 한국 RA팀과 마케팅팀 사이의 일정 갈등이 가장 심해지는 영역입니다. 신고 판단 구조와SR 실무 변화는 22편에서 집중적으로 다루겠습니다.
변화4: 소비자 정보접근과 리스크 커뮤니케이션 강화
소비자청은 판매 중인 기능성표시식품의 안전성ㆍ기능성에 관한 과학적 근거 등의 정보가 소비자 눈높이에서 쉽고 분명하게 제공되도록 웹사이트DX 대응을 강화하고 있습니다. 또한 기능성표시식품 섭취 시 의약품과의 상호작용, 과잉섭취 등의 리스크에 대한 소비자 교육도 강화하고 있습니다.
아울러 도도부현 등에 제공된 건강피해 정보가 후생노동성에 집약되어 식품위생법상 조치 필요성을 검토하는 구조가 보다 분명해졌습니다. 후생노동성 산하에 “기능성표시식품 등의 건강피해정보 대응에 관한 소위원회”가 설치되어, 수집된 건강피해 사례를 의학적ㆍ역학적으로 분석ㆍ평가한 뒤 정기적으로 결과를 공표하는 체계가 운영되고 있습니다.
일본 정부가 기능성표시식품에 대한 사후 감시를 느슨하게 가져갈 신호는 전혀 보이지 않습니다. 소비자가 신고DB를 통해 과학적 근거를 직접 확인할 수 있는 구조가 강화되면서, “대충 신고해서 번호만 받으면 된다”는 접근은 시장에서도 통하지 않게 되고 있습니다.
한국 수출사가 놓치기 쉬운3가지 포인트
포인트1: “한국GMP가 있으니 일본도 되겠지“
제가 상담한 한 프로바이오틱스OEM 업체는 한국 건강기능식품GMP 인증을 보유하고 있었고, 일본 파트너로부터 “GMP 적합 확인서를 달라”는 요청을 받았습니다. 한국GMP 인증서를 번역해서 보냈더니, 일본 파트너가 “이걸로는 안 된다”고 회신했습니다.
이유는 간단합니다. 일본 고시(내각부 고시 제108호)는 한국 건강기능식품GMP와 체계가 다릅니다. 가장 눈에 띄는 차이는 조직 구조입니다. 일본 고시는 총괄책임자ㆍ제조관리책임자ㆍ품질관리책임자의 3자 분리를 요구하는데, 총괄책임자는 품질관리책임자를 겸할 수 있지만 제조관리책임자를 겸할 수 없고, 제조관리책임자와 품질관리책임자도 서로 겸직이 불가합니다. 또 제품표준서ㆍ제조관리기준서ㆍ품질관리기준서ㆍ수순서4종의 문서 체계를 요구하고, 밸리데이션, 일탈관리, 변경관리, 품질정보관리, 자기점검 등의 절차를 각각 수순서에 기재하도록 되어 있습니다.
한국GMP를 갖추고 있다면 출발점은 분명히 유리합니다. 하지만 “자동으로 적합”하지는 않습니다. 갭 분석부터 시작해야 합니다. 21편에서 고시 조문과 한국GMP 기준의 항목별 대조표를 제시하겠습니다.
포인트2: “한국에서 개별인정형 원료니까 일본에서도 기존 성분이겠지”
한 건강기능식품 원료사가 자사의 프로바이오틱스 균주를 일본 기능성표시식품으로 신고하려 했습니다. 한국에서는 식약처 개별인정형으로 허가받은 원료인데, 일본 소비자청에서는 “신규 기능성관여성분”으로 분류되어 신고 확인기간이120영업일로 늘어났습니다. 마케팅팀이 잡아둔 출시 일정이 반년 가까이 밀린 겁니다.
일본 소비자청의 신규/기존 판단은 한국 식약처와 완전히 별개입니다. 일본에서 이미 신고ㆍ공표된 기능성관여성분과 동일한 성분이라면 기존 성분으로 취급되지만, 그렇지 않으면 신규로 분류됩니다. 신규 성분의 경우 소비자청이 전문가 의견을 듣는 절차가 추가되므로, 확인기간이120영업일로 늘어날 수 있습니다.
따라서 일본 진출을 계획할 때는 출시 일정을 잡기 전에 먼저 “우리 원료가 일본에서 기존 성분인지 신규 성분인지”를 확인하는 것이 필수입니다. 이 판단 구조와 시간 관리 전략은22편에서 상세히 다루겠습니다.
포인트3: “신고 번호를 받으면 끝“
많은 한국 기업이 기능성표시식품 신고 번호를 받는 순간 “일본 진출 완료”라고 생각합니다. 하지만 개정 제도에서는 신고 이후의 의무가 이전과 비교할 수 없을 만큼 강화되었습니다.
신고자는 연1회 자기점검을 실시하고 그 결과를 신고DB를 통해 보고해야 하며, 보고 내용은 공표 대상입니다. 점검 항목에는 기능성관여성분의 안전성ㆍ기능성에 관한 새로운 지견이 보고되었는지, 생산ㆍ제조ㆍ품질관리 사항이 준수되고 있는지, 건강피해 정보 수집ㆍ제공 체계가 가동되고 있는지 등이 포함됩니다. 기한 내 보고하지 않으면 해당 신고는 기능성표시식품으로서의 요건을 결하게 되며, DB상 변경신고ㆍ판매상황 갱신ㆍ철회 등 후속 작업도 제한됩니다.
건강피해 정보 수집ㆍ제공 체계 역시 상시 가동해야 합니다. 이를 이행하지 않으면 기능성표시식품으로서의 요건을 갖추지 못한 것으로 취급될 수 있으며, 식품표시법에 근거한 지시ㆍ명령 등 행정조치가 가능합니다.
일본 파트너가 신고자인 경우에도, 자기점검 보고 기한이 도래했거나 임박했는지, 보고 체계가 설계되어 있는지를 확인해야 합니다. “파트너가 알아서 하겠지”라는 가정은 위험합니다. 신고자의 의무 불이행은 곧 해당 제품의 판매 리스크로 직결되기 때문입니다. 사후관리SOP 설계와 역할분담 방법은 24편에서 다루겠습니다.
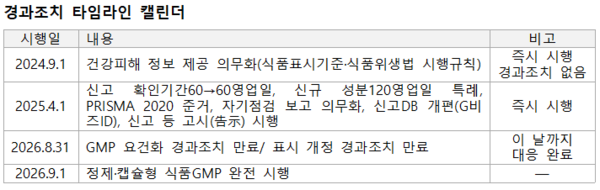
이 캘린더에서 한국 기업이 가장 역산해야 할 날짜는 2026년 9월 1일입니다. 또한 일본 식품표시 전반에서는 영양소 기준값 개정(2028년 3월 31일 경과조치 만료), 영양강화 목적 첨가물 표시 의무화(2030년 3월 31일 경과조치 만료) 등 추가 일정이 있으므로, 중장기적으로 일본향 제품 전반의 표시 점검이 필요합니다.
라벨 프로젝트에서 운영 프로젝트로
지금까지 일본 기능성표시식품은 많은 한국 기업에게 “라벨을 일본어로 만들고SR을 붙이는 프로젝트”였습니다. 일본 파트너가 신고를 대행하고, 한국 본사는 원료와 완제품을 보내면 되는 구조에 익숙했습니다.
하지만 홍국 이후의 제도 개편은, 기능성표시식품을 “원료 안전성→제조관리→신고→표시→판매 후 감시”까지 아우르는 운영 체계로 바꿔놓았습니다. 제조사가 GMP를 갖추고, 건강피해 정보가 신고자에게 흘러가는 경로를 설계하고, 연1회 자기점검 결과를 보고하고, 그 결과가 공표되는 체계를 운영하는 것이 “기능성표시식품을 유지하는 비용”이 된 것입니다.
이 시리즈의 핵심 메시지는 기존Prop 65 시리즈와 같습니다. “그냥 붙이기/피하기가 아니라, 계산하고 설명하고 문서화하는 것이 진짜 경쟁력.” 일본 기능성표시식품에서도 마찬가지입니다. 제도를 이해하고, 체계를 갖추고, 문서로 증명하는 기업이 살아남습니다.
21편에서는 GMP 의무화의 대상 범위 판정부터 시작합니다. “우리 제품이 대상인가”를 먼저 확인하고, 일본 고시(내각부 고시 제108호)가 요구하는 제조관리ㆍ품질관리 체계를 한국 건강기능식품 GMP와 대비해서 풀겠습니다.
자주 받는 질문(FAQ)
Q1. 일반식품으로 일본에 수출하고 있는데, 이번 제도 개편이 우리에게도 해당되나요?
기능성표시식품으로 신고하지 않고 일반 가공식품으로 수출하는 경우, 이번 개편의 직접 대상은 아닙니다. 다만 일본 바이어가 향후 기능성표시식품 전환을 요청하거나, 제품 패키지에 건강 관련 표현을 넣고 싶다면 이 시리즈 전체를 미리 파악해 두시는 것이 좋습니다. 일반식품에 기능성을 암시하는 표현을 쓰면 건강증진법ㆍ부당경품류 및 부당표시방지법(景品表示法) 위반 리스크가 있습니다.
Q2. 한국에서 건강기능식품으로 허가받은 제품을 일본에서 기능성표시식품으로 바로 신고할 수 있나요?
바로는 어렵습니다. 한국 식약처의 건강기능식품 허가와 일본 소비자청의 기능성표시식품 신고는 별개의 제도입니다. 한국에서 인정받은 기능성 원료라 해도 일본에서는 신고 요건에 맞는 안전성ㆍ기능성 근거(SR 또는 RCT), 분석방법, 표시안 등을 자체적으로 갖춰야 합니다. 다만 한국에서 축적한 시험 데이터나 논문은SR 작성 시 활용할 수 있으므로, 완전히 “처음부터 다시”는 아닙니다.
Q3. 이번 개편에서 가장 긴급한 것은 무엇인가요?
이미 기능성표시식품으로 신고된 제품을 보유한 기업이라면, 건강피해 정보 제공 의무와 자기점검등 보고 체계를 가장 먼저 점검해야 합니다. 건강피해 정보 제공 의무는 2024년 9월 1일부터 시행되었고, 자기점검등 보고는 1년 1회 정기적으로 이루어져야 하며 그 결과는 공표 대상이 됩니다. 아직 신고 전이라면, 2026년 9월 GMP 완전 시행을 역산하여 자사 제품이GMP 적용 대상인지, 제조ㆍ품질관리 체계를 어떻게 입증할지부터 점검하는 것이 우선입니다.
Q4. 일본 현지 파트너(수입업자)가 신고자인 경우, 한국 제조사에게도 의무가 있나요?
법적 의무의 주체는 신고자인 일본 현지 파트너입니다. 다만 소비자청 Handbooks와 Q&A는, 천연추출물 등을 원재료로 하는 정제ㆍ캡슐형 식품의 경우 GMP 기준에 맞게 제조ㆍ가공되도록 확보하는 책임이 신고자에게 있다고 설명합니다. 결국 일본 파트너는 한국 제조사에게GMP 적합 자료, 원료 안전성 자료, 제조ㆍ품질관리 기록, 건강피해 대응SOP 등을 요구할 수밖에 없습니다. 즉, 법적 의무는 일본 파트너에게 있지만 실무 준비 부담은 한국 제조사에도 직접 미칩니다.
Q5. 일본에서 이미 많이 쓰는 원료인데도 120영업일 검토 대상이 될 수 있나요?
그럴 수 있습니다. 일본 기능성표시식품 신고는 기본적으로 판매 60영업일 전 신고가 원칙이지만, 소비자청이 자료 확인에 특히 시간이 필요하다고 판단하는 경우에는120영업일 구조가 적용될 수 있습니다. 특히 기존에 공표된 적 없는 기능성관여성분, 또는 기존 성분이라도 공표된 적 없는 조합은 120영업일 검토 대상으로 이어질 가능성이 있습니다. 따라서 한국에서 익숙한 원료인지보다, 일본 기능성표시식품DB에서 해당 성분이나 조합이 이미 공표된 적이 있는지를 먼저 확인하는 것이 실무상 중요합니다.
관련기사
☞ 네이버 뉴스스탠드에서 식품저널 foodnews를 만나세요. 구독하기 클릭





_(1)(1).jpg)
건우에프피.jpg)

